

由于能源危机和碳排放的增加,开发清洁、可持续的能源迫在眉睫。作为氢气储存和运输的高效载体,氨是实现零碳排放社会的理想清洁能源载体。而开发高催化活性、高稳定性的电化学氮还原反应 (NRR) 催化剂是一项重大挑战。
山西大学的研究团队通过向LaFeO3(LF)钙钛矿的B位掺杂Cu,创造出了一种新型电催化剂LaCu0.1Fe0.9O3−δ(LCuF),旨在应用于氮气还原反应(NRR)。当这种催化剂被用作质子陶瓷电解池(PCEC)的阴极材料时,它展现出了出色的NRR催化性能及长期的稳定性。研究的关键发现在于Cu和Fe之间的协同效应显著增强了LCuF的NRR活性。这种协同效应的工作机制是电子通过Fe—O2−δ—Cu链进行转移,导致在Fe位点产生了更多的Fe4+,而在Cu位点则形成了更多的Cu+。这一过程加速了电子的转移速率,进而提高了NRR的反应速率。同时,Cu+的增多还引发了其周围产生更多的氧空位(OV)。值得注意的是,Fe4+和OVs都是缺电子的物种,它们能够捕获在吸附氮分子的反键轨道中的亚稳态电子,从而有效地活化N2。这项研究不仅揭示了Cu和Fe在LCuF催化剂中的协同作用机制,还为开发高效的NRR电催化剂提供了一种新的、可行的策略。
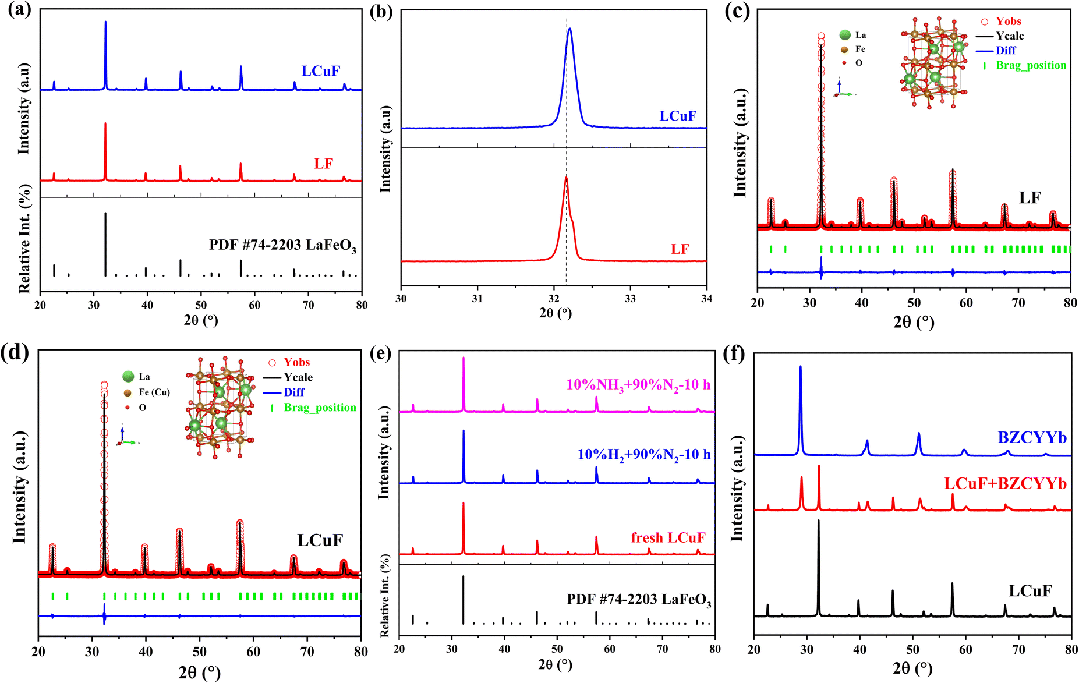
图 1(a)制备好的 LF 和 LCuF 的 XRD 图案;(b)30–34° 下 LF 和 LCuF 的放大 XRD 图案;(c)LF 和(d)LCuF 的 Rietveld 细化和结构模型;(e)在 700°C 下暴露于 10%H2+90%N2 和 10%NH3+90%N2后的新鲜和处理过的 LCuF 粉末的 XRD 图案;(f)LCuF、BZCYYb 和 BZCYYb–LCuF(质量比 = 1:1)的 XRD 图案。
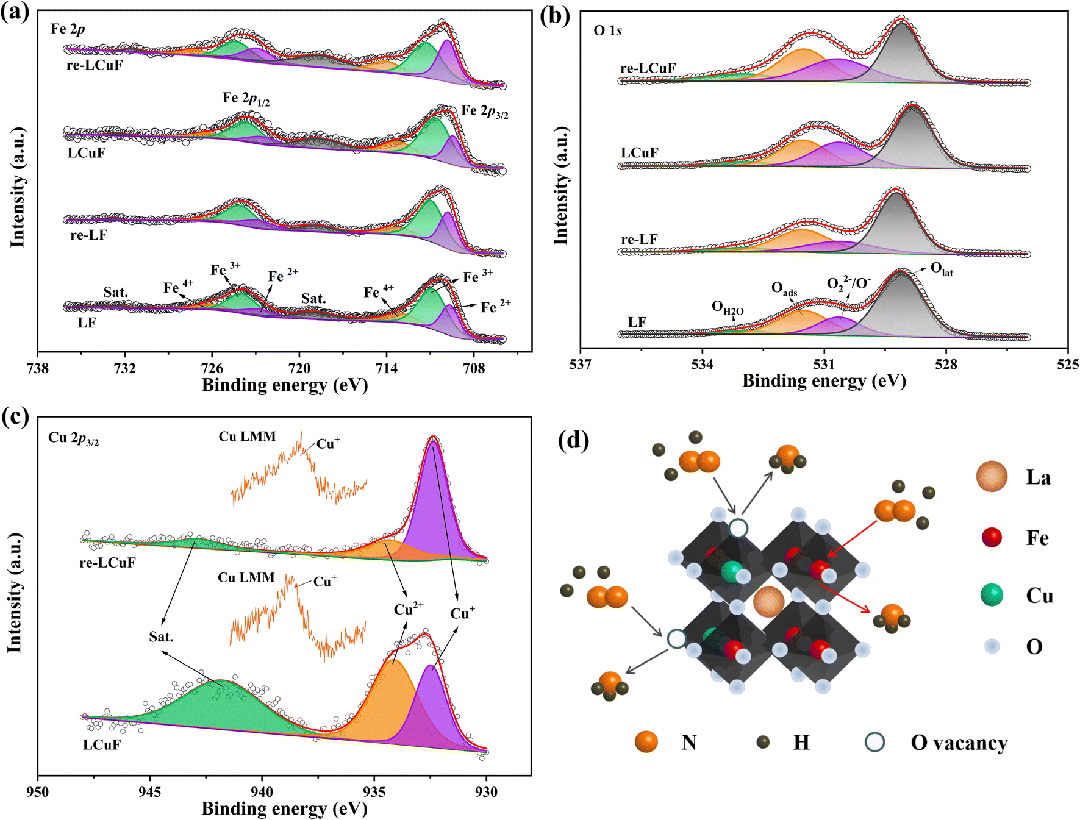
图 2 LF、re-LF、LCuF 和 re-LCuF 的 XPS 光谱:(a) Fe 2p、(b) O 1s 和 (c) Cu 2p 3/2(插图:Cu LMM)光谱;(d) 活性位点 NRR 示意图。
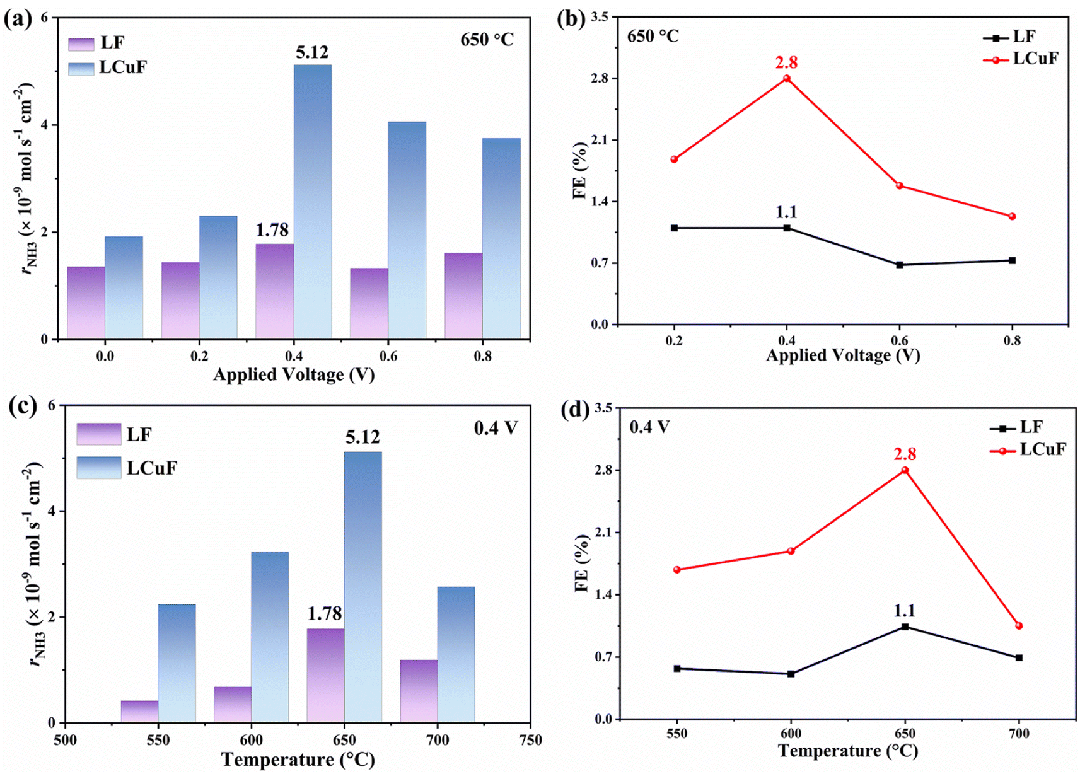
图 3 (a)不同电压和 650°C 下 LF 基和 LCuF 基电池的氨合成速率和(b)FE;(c)不同温度和 0.4 V(vs. OCV)下 LF 基和 LCuF 基电池的氨合成速率和(d)FE。
在550至750°C的温度区间内,对LF基电池和LCuF基电池进行了线性扫描伏安(LSV)测试。对于 LF 和 LCuF 基电池,电流密度均随温度和施加电压的升高而增大。在相同温度和施加电压下,LCuF 基电池的电流密度高于 LF 基电池。由于两个电池中的复合阳极和电解质相同,电流密度的变化主要是由不同阴极材料的 NRR 催化活性不同引起的。这清楚地表明 LCuF 的 NRR 活性高于 LF。
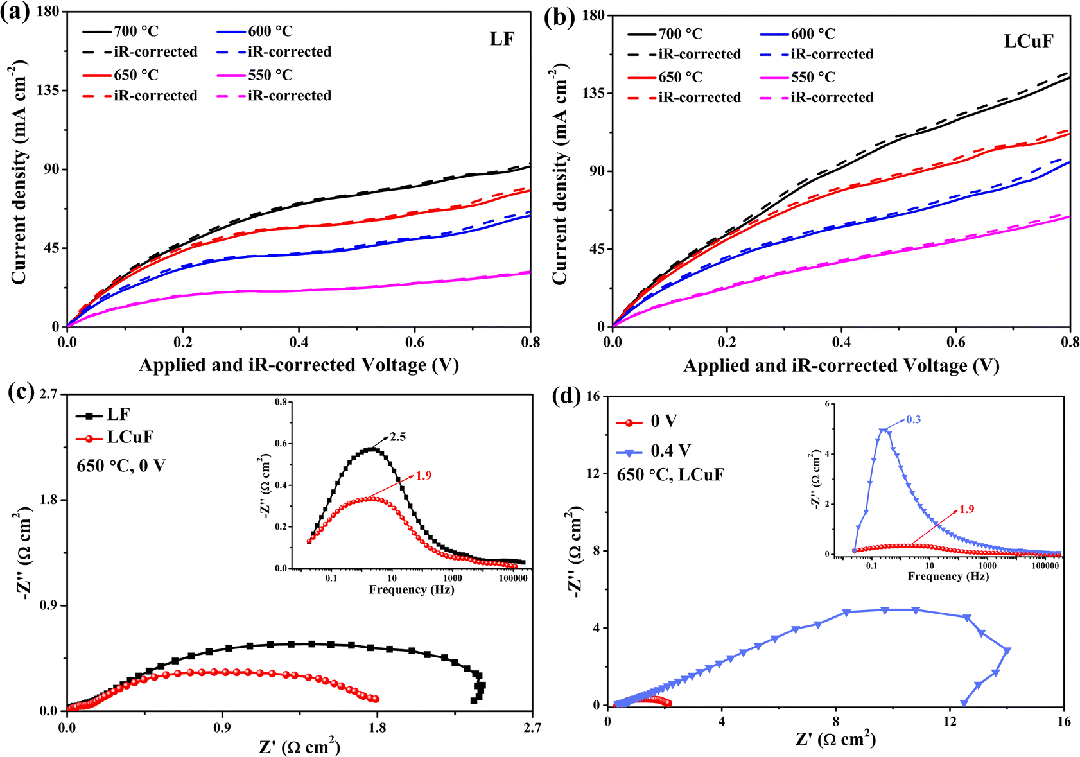
图 4 不同温度下 (a) LF 基和 (b) LCuF 基电池的 LSV 曲线;650°C 和 0 V 下 (c) LF 基和 LCuF 基电池的 Nyquist 和 Bode 曲线以及 650°C 和不同电压 (0 V 和 0.4 V ( vs. OCV)) 下 (d) LCuF 基电池的 Nyquist 和 Bode 曲线。
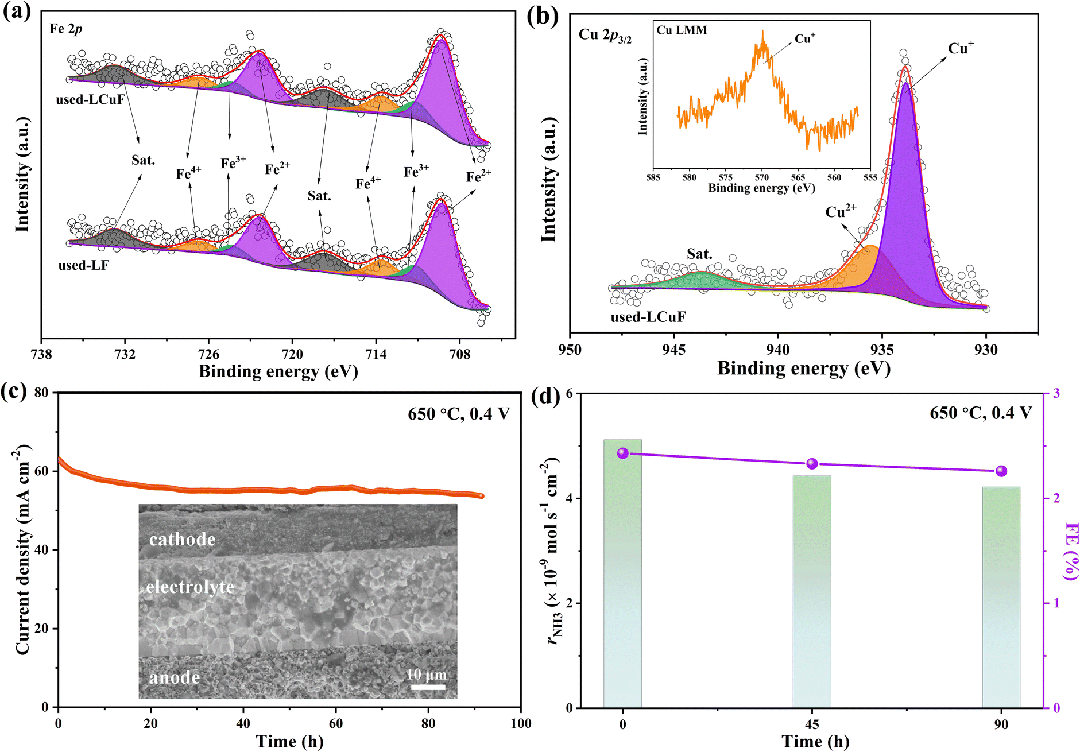
图 5 长期 NRR 测试后 LF 和 LCuF 基电池阴极部分的 XPS 光谱:(a) Fe 2p 和 (b) Cu 2p 3/2(插图:Cu LMM)光谱。(c) 650°C 和 0.4 V 下 LCuF 基电池的长期稳定性测试。插图:90 小时测试后 LCuF 基电池的横截面 SEM 图像;(d) 氨合成速率和 FE 随时间的变化。