具有肿瘤微环境多模态成像和协同治疗作用的金属调控克酮酸菁染料在肿瘤诊疗中展现出巨大潜力。然而,其结构优化不理想总会削弱近红外荧光光声 (NIRF/PA) 成像和光热治疗 (PTT) 的功效。
在此,山西大学阴彩霞、南方医科大学周春琼、瓦伦西亚大学Jorge González-García联合团队筛选出家族中含有两个吲哚基团、具有较好NIRF/PA成像和PTT的克酮酸菁染料,连接两个吗啉环,得到溶酶体靶向和Fe3+调控剂CR-736。建立的CR-736-Fe3+纳米平台可准确递送至乳腺肿瘤部位,在酸性较低的溶酶体微环境中释放CR-736和Fe3+,激活pH响应的NIRF/PA/磁共振成像和PTT。此外,铁死亡通过肿瘤细胞中Fe3+的积累消耗GSH和H2O2产生羟基自由基和脂质过氧化物,导致热休克蛋白表达受抑制,PTT随之恢复。 PTT、铁死亡和化学动力学的协同治疗在肿瘤溶酶体酸性微环境中得到最大程度的优化,并在体外和小鼠肿瘤模型中得到验证。本研究为设计优良独特的克酮酸菁纳米平台、协同多种肿瘤诊疗方法以及进一步优化肿瘤微环境中的诊疗效果开辟了新途径。相关研究成果发表于《ACS Appl. Mater. Interfaces》上。
图文解析
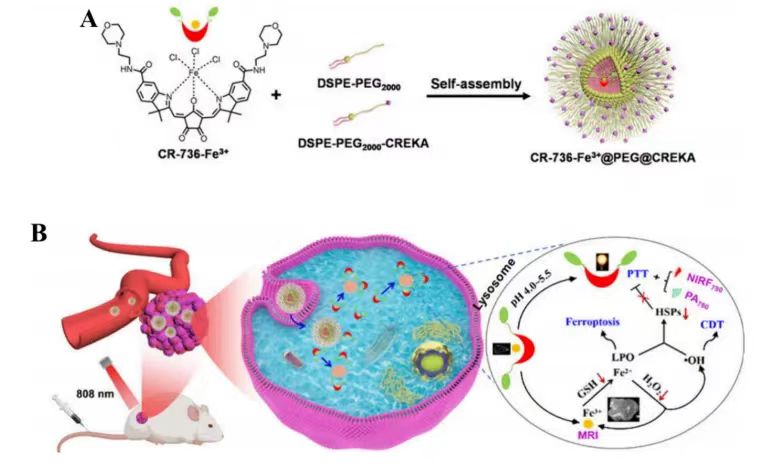
方案 1. (A) CR-736-Fe3+@PEG@CREKA NPs制备示意图;(B) CR736-Fe3+@PEG@CREKA NPs 示意图,显示 pH 响应性 NIR/PA/MRI 成像以及 PTT、铁死亡和 CDT 对乳腺癌的协同作用。
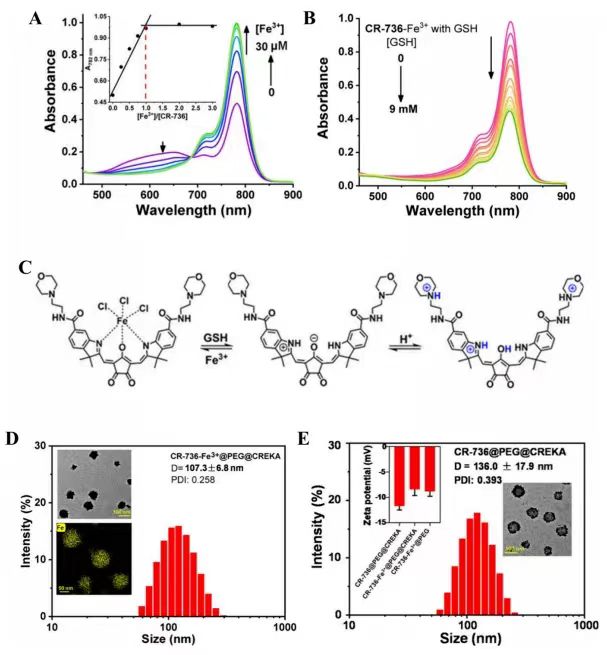
图 1. (A) 在Fe3+ 离子 (0-30 μM) 存在下 CR-736 (10 μM) 的紫外可见光谱。插图:不同摩尔比 [Fe3+]/[CR-736]下 782 nm 处的吸光度值。(B) 在 GSH (0-9 mM) 存在下 CR-736-Fe3+ (10 μM) 的紫外可见光谱。(C) CR-736 和 CR-736-Fe3+在 Fe3+ 和 GSH 中的结构转化以及酸性环境中 CR-736 的 pH 响应。(D) DLS 对CR-736-Fe3+@PEG@ CREKA NPs 的尺寸分布进行分析。插图:它们的 TEM 照片(上;比例尺,100 nm)和铁元素映射(下;比例尺,50 nm)。 (E) 通过 DLS 确定的 CR-736@PEG@CREKA NPs 的尺寸分布。插图:三个纳米粒子的ζ电位(左)及其 TEM 照片(右;比例尺,100 nm)。
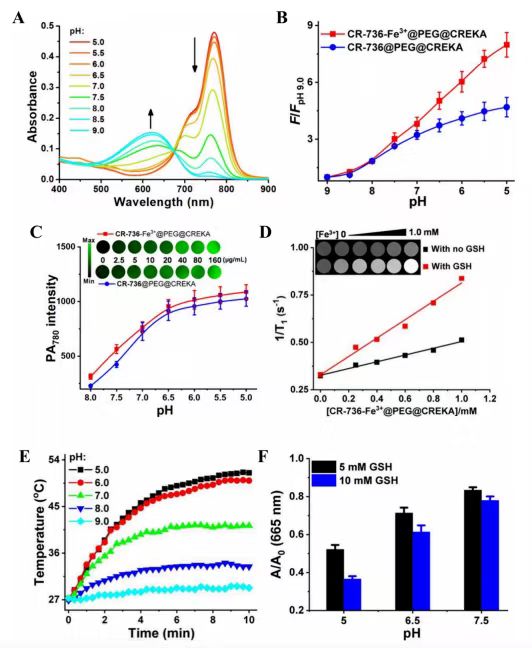
图 2. (A) 不同 pH 值下 CR-736-Fe3+@PEG@CREKA NPs(8 μg/mL)的紫外可见光谱。 (B) 不同 pH 值(5.0-9.0)和λex/λem= 765 nm/ 792 nm 下 CR736-Fe3+@PEG@CREKA NPs(8 μg/mL)和 CR-736@PEG@CREKA NPs(8μg/mL)的荧光强度比及其在 pH 9.0 下的荧光强度。 (C) 不同 pH 值(5.0-8.0)下 CR-736-Fe3+@PEG@CREKA NPs(40 μg/mL)和 CR-736@PEG@ CREKA NPs(40μg/mL)的 PA780 强度。插图:pH 值为 6.5 时0-160 μg/mL CR-736-Fe3+@PEG@CREKA NPs 和 CR-736@ PEG@CREKA NPs 的 PA780 图像。(D) pH 值为 5.0 时不同 CR-736-Fe3+@PEG@CREKA浓度(不含和含有 GSH(6 mM))的 T1 加权 MR 弛豫时间的倒数。(E) 辐射(808 nm,1.0 W/cm2)下不同 pH 值下 CR-736-Fe3+@PEG@CREKA(6.25μg/mL)的温度。 (F) 在三种 pH 值(5.0、6.5和 7.5)下,5 μg/mL MB、5 或10 mM GSH 和 30 mM H2O2 与 60 μg/mL CR736-Fe3+@PEG@CREKA NPs 在665 nm 处的吸光度比 A/A0。
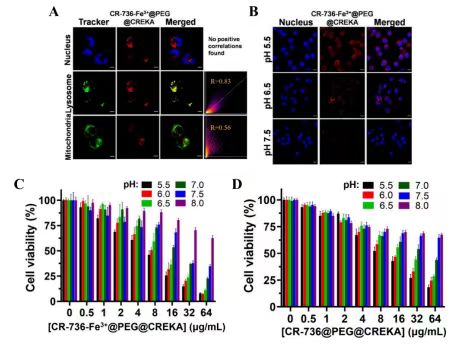
图 3. (A) 4T1 细胞与 CR-736Fe3+@PEG@CREKA NPs (20 μg/mL) 孵育后分别用 Hoechst 33342、Lyso-Tracker Green 和 Mito Tracker Green 染色后的 CLSM 图像。比例尺:5 μm。 (B) 4T1 细胞在不同 pH 值下与 CR-736-Fe3+@PEG@CREKA NPs (20 μg/mL) 孵育后的荧光图像,其中蓝色通道 (λex = 405 nm) 和红色通道 (λex = 633 nm)。比例尺:20 μm。 (C、D)不同浓度和 pH 值的 CR-736-Fe3+@PEG@ CREKA NPs 和 CR-736@PEG@CREKA NPs 对 4T1 细胞的光热细胞毒性(808 nm、1.0 W/cm2、10 分钟)。
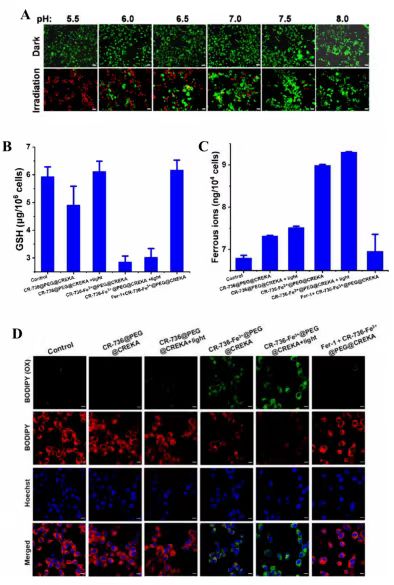
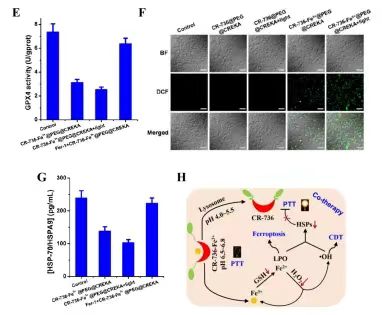
图 4. (A) 用CR-736-Fe3+@PEG@CREKA NPs(32 μg/mL,pH 5.5−8.0)在黑暗和光照(808 nm,1.0 W/cm2,10 分钟)处理的 4T1 细胞的 Calcein-AM/PI 荧光图像。比例尺:20 μm。(B) 不同处理后 4T1 细胞中的 GSH 和(C)亚铁离子。(D) 不同处理后 4T1 细胞的共聚焦荧光图像。BODIPY 呈现红色荧光,BODIPY (OX) 呈现绿色荧光,Fer-1 是铁死亡的抑制剂。比例尺:10 μm。(E)不同处理后 4T1 细胞中 GPX4 的酶活性。(F) 不同处理后 4T1 细胞中 ROS 生成的共聚焦图像。比例尺:50 μm。(G) 不同处理后 4T1 细胞中 HSP 的表达水平。(H) PTT 增加、铁死亡和 CDT 协同作用的潜在机制。
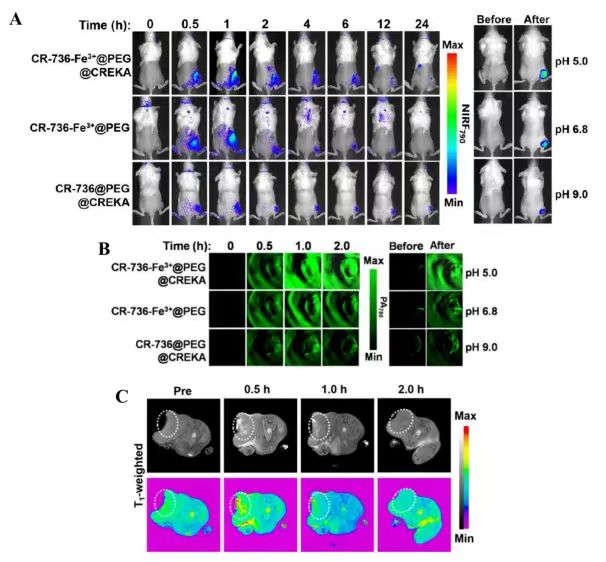
图5. (A)肿瘤小鼠尾静脉注射CR-736-Fe3+@PEG@CREKA NPs(5 mg/kg)、CR736-Fe3+@PEG NPs(5 mg/kg)、CR-736@PEG@CREKA NPs(5 mg/kg)后不同时间点的NIRF790图像(左),肿瘤小鼠瘤内注射CR-736-Fe3+@PEG@CREKA NPs后不同pH值下的NIRF790图像(右)。(B)肿瘤小鼠注射CR-736-Fe3+@PEG@CREKA NPs(5 mg/kg)、CR-736-Fe3+@PEG NPs(5 mg/kg)、CR-736@PEG@CREKA NPs(5 mg/kg)后不同时间点的PA780图像(左);肿瘤小鼠注射CR-736-Fe3+@PEG@CREKA NPs后不同pH值下的PA780图像(右)。(C)肿瘤小鼠注射CR-736-Fe3+@PEG@CREKA NPs(5 mg/kg)后不同时间点的T1加权MRI图像。
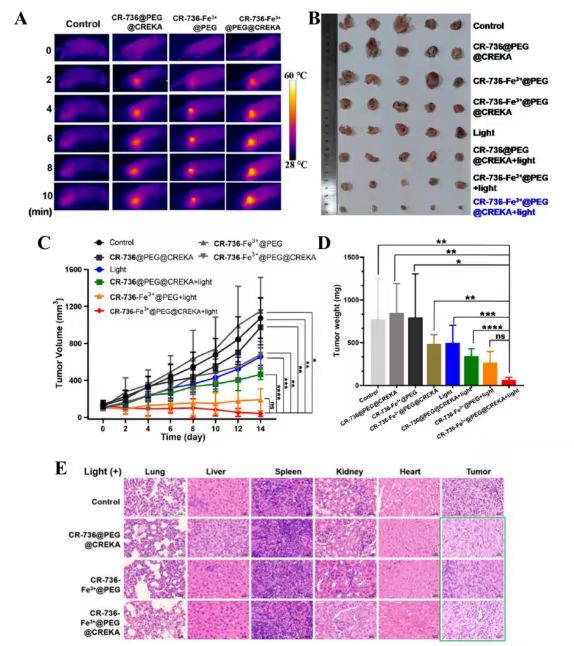
图6. (A) 小鼠肿瘤内注射CR-736-Fe3+@PEG@CREKA NPs (1 mg/kg)、CR736-Fe3+@PEG NPs (1 mg/kg) 和CR-736@PEG@CREKA NPs (1 mg/kg)后不同照射时间 (808 nm, 1.0 W/cm2 ) 后肿瘤区域的温度。 (B) 不同治疗后第14天的肿瘤照片。 (C, D) 不同治疗后肿瘤生长随时间 (C) 和第14天重量 (D) 的曲线。Ns:无显著性、*p ≤ 0.05、**p ≤0.01、***p ≤ 0.001 和****p ≤ 0.0001。 (E) 不同治疗后照射中主要器官的H&E染色照片。比例尺:20 μm。